INTRODUCCIÓN
AL METABOLISMO
1. EL METABOLISMO
El
conjunto de intercambios de energía y transformaciones de la materia que tienen
lugar en el interior de la célula debido a procesos químicos constituyen el
metabolismo. Entre los objetivos básicos del metabolismo figuran la destrucción
o degradación de moléculas y la construcción o síntesis de ellas.
Sin
duda, las células son los laboratorios más sofisticados que existen. Para que
las diferentes rutas metabólicas operen coordinadamente, es imprescindible un
control riguroso mediante diferentes enzimas específicos, y que las
distintas rutas se lleven a cabo, en muchos casos, en compartimentos celulares
separados (orgánulos celulares).
2.
ENZIMAS
Las reacciones que tienen lugar en los organismos no pueden ser violentas, lo cual se consigue gracias a la existencia de los biocatalizadores, entre los cuales el lugar más destacado lo ocupan los enzimas.
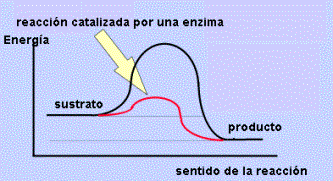
Para
que una reacción se lleve a cabo es necesario que la/s sustancia/s que van a
reaccionar (sustratos) reciban una determinada cantidad de energía que las
active, denominada energía de activación. Los catalizadores son pues
aquellas sustancias que, al disminuir las necesidades de energía de activación
de una reacción, la facilitan y la aceleran.

Los
catalizadores no intervienen en la reacción que catalizan, de tal manera que,
una vez terminada ésta, quedan libres y pueden volver a ser utilizados, no se
consumen durante la reacción.
La
mayoría de los enzimas conocidos
son proteínas de gran solubilidad. Algunos otros son ácidos ribonucleicos
(ARN).
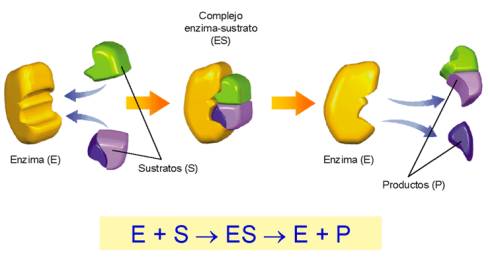
Los
enzimas son específicos, es decir, cada uno de ellos actúa solamente
sobre un determinado sustrato. Actualmente se considera que la especificidad
enzimática radica en la naturaleza de los aminoácidos de fijación del centro
activo. Una vez realizada la fijación del sustrato a dichos aminoácidos,
el enzima posee una considerable libertad para modificar su forma y amoldarse
parcialmente sobre el sustrato, de tal manera que el sitio catalítico quede
correctamente situado para actuar.
La velocidad de la reacción enzimática puede verse modificada por diversos factores:
ü
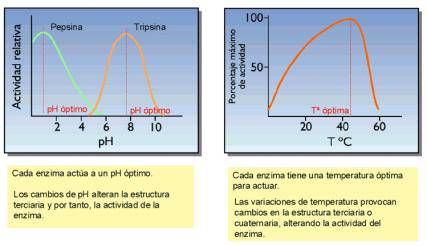
Temperatura:
a medida que ésta aumenta, también aumenta la actividad enzimática hasta
llegar a un punto óptimo en que dicha actividad es la máxima. Pero si sigue
elevándose la temperatura, llega un momento en que el enzima se desnaturaliza y
cesa su actividad.
ü pH: un enzima sólo actúa dentro de unos límites de pH. Entre ellos está el llamado pH óptimo en el que la reacción alcanza su máxima eficacia. Sobrepasados los límites de pH, el enzima se desnaturaliza.
ü
Sustancias inhibidoras:
se trata de compuestos químicos que logran inhibir en menor o mayor medida,
incluso anular, la actividad de un enzima sin destruirlo. Este hecho las
distingue de las sustancias inactivadoras. La acción inhibidora puede ser de
dos tipos: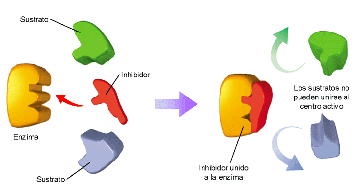
Inhibición competitiva: se debe a que el inhibidor tiene una molécula tan parecida a la del sustrato que logra unirse al centro activo del enzima, el cual, como no puede actuar sobre él, permanece unido sin separarse impidiendo que el sustrato ocupe el centro activo.
Inhibición no competitiva: se debe a que el inhibidor se une al enzima de tal manera que impide que el sustrato llegue al centro activo o bien, se une al complejo enzima-sustrato impidiendo la separación.
Tanto la inhibición competitiva como la no-competitiva son reversibles. Sin embargo existe también una inhibición irreversible o envenenamiento que tiene lugar cuando el inhibidor se fija permanentemente al centro activo del enzima y por tanto, lo inutiliza.
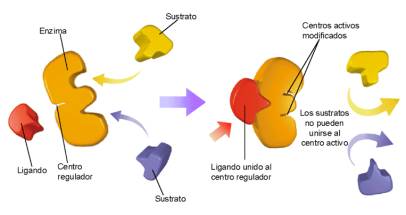
ü Alosterismo: es la propiedad que poseen algunos enzimas (llamados alostéricos) de modificar su actividad cuando su estructura terciaria se transforma por una molécula orgánica (efector alostérico) que se une en un punto diferente del centro activo denominado centro alostérico.
Los enzimas se clasifican en 6 grupos en función de la acción que realizan. Para denominar un enzima se utiliza generalmente el nombre del sustrato sobre el que actúa con la terminación -asa (por ejemplo, sacarasa). Algunos enzimas, sin embargo, siguen conservando su nombre antiguo, por ejemplo, tripsina.

3. PROCESOS CATABÓLICOS Y ANABÓLICOS
Todos los procesos metabólicos se pueden clasificar en dos tipos: procesos anabólicos, o de síntesis; y procesos catabólicos, o de degradación.
§ Catabolismo.
Son
reacciones de descomposición de moléculas complejas en otras más simples.
Tienen dos finalidades: suministrar energía (al romperse los enlaces químicos)
necesaria para cualquier trabajo celular, y aportar pequeñas moléculas para
los procesos de síntesis.
El
catabolismo se puede iniciar con la descomposición de muy diferentes sustancias
orgánicas, pero, al final, la mayoría de las rutas catabólicas confluyen en
la respiración celular, a través de la cual los compuestos orgánicos
se terminan por degradar en sustancias inorgánicas.
§ Anabolismo.
Son reacciones de síntesis de moléculas grandes a partir de moléculas
sencillas. Permiten el crecimiento, la regeneración de estructuras o el
empaquetamiento y almacén de sustancias de reserva. En estas reacciones se
crean nuevos enlaces químicos y, por tanto, requieren un aporte de energía.
El
anabolismo se inicia con la síntesis de los primeros compuestos orgánicos a
partir de sustancias inorgánicas, mediante la fotosíntesis o la quimiosíntesis.
Esos primeros pasos anabólicos sólo los pueden realizar los organismos autótrofos.
Luego, a partir de moléculas orgánicas simples, se formarán, mediante
diferentes rutas anabólicas, todos los componentes orgánicos de los seres
vivos.
4. ENERGÍA METABÓLICA
La
“moneda energética” de la célula es el ATP, que está formado por
adenina, ribosa y tres grupos fosfatos. Contiene enlaces de alta energía entre
los grupos fosfato; al romperse dichos enlaces se libera la energía almacenada.
La
hidrólisis del ATP libera la energía contenida en el enlace fosfato.
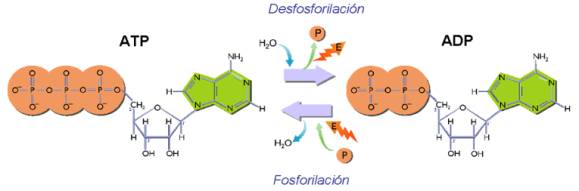
La fosforilación del ADP es la síntesis de ATP. En las células se
utilizan dos mecanismos para sintetizar ATP:
§
Fosforilación a nivel
de sustrato: Se utiliza la
energía liberada por una reacción exotérmica para fosforilar ADP y sintetizar
ATP.
§
Fosforilación en el
transporte de electrones: se
produce mediante el enzima ATP-sintetasa en la mitocondria y el cloroplasto.
Cuando ocurre en las mitocondrias se denomina fosforilación oxidativa y si
ocurre en los cloroplastos fosforilación fotosintética o fotofosforilación.
Muchas de las reacciones del catabolismo suponen la oxidación de un
sustrato, lo cual libera electrones. Por el contrario, el anabolismo
frecuentemente consiste en reacciones de reducción que requieren electrones.
Los electrones son transportados mediante coenzimas transportadores de electrones, como el NAD (nicotinamida-adenina-dinucleótido) o el FAD (flavina-adenina-dinucleótido), que llevan electrones de un punto a otro de la célula de un modo similar a como el ATP transporta la energía. Cuando uno de estos coenzimas se encuentra cargado de electrones (oxidado) se dice que tiene poder reductor, puesto que al liberarse de los electrones podrá reducir a otro compuesto.
5. TIPOS DE ORGANISMOS SEGÚN SU METABOLISMO
Teniendo
en cuenta la fuente de energía y la de carbono, los seres vivos se agrupan en:
|
TIPO DE ORGANISMO |
FUENTE DE ENERGÍA |
FUENTE DE CARBONO |
ORGANISMOS |
|
Fotolitótrofo (fotoautótrofo) |
Luz solar |
CO2 |
Vegetales, bacterias fotosintéticas |
|
Fotoorganótrofo (fotoheterótrofo) |
Luz solar |
Compuestos orgánicos |
Bacterias purpúreas |
|
Quimiolitótrofo (quimioautótrofo) |
Reacciones químicas |
CO2 |
Bacterias nitrificantes |
|
Quimioorganótrofo (quimioheterótrofo) |
Reacciones químicas |
Compuestos orgánicos |
Animales y hongos |
Naturalmente,
muchas de las reacciones químicas, tanto anabólicas como catabólicas,
implican transformaciones energéticas, y los procesos que liberan energía (en
general los catabólicos) se acoplan a los que la consumen (en general los anabólicos).
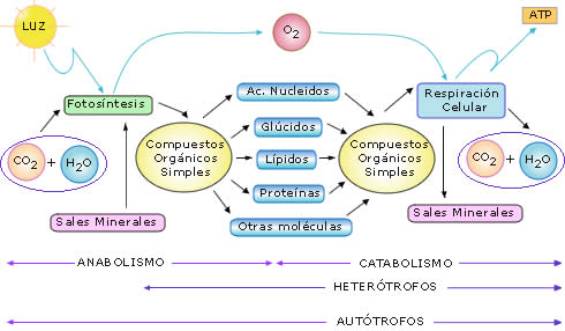
Esquema de los principales procesos metabólicos
realizados por los organismos autótrofos y heterótrofos