Mol�culas esf�ricas:
Enlaces del Diamante
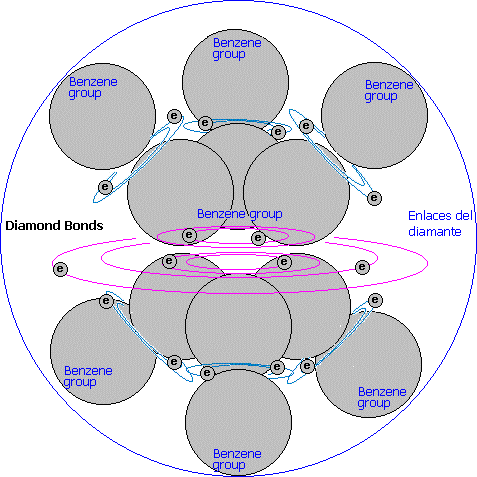
La primera cuesti�n a considerar en el diamante es que su dureza y estructura cristalina se deban a que cada diamante forma una sola mol�cula de carbono.
Al mantenerse unidos todos sus �tomos por enlaces covalentes en sus dos direcciones (Cis-Trans)
se constituyen en una sola mol�cula tridimensional que le da su dureza y su estado cristalino.
Consta de grupos hexas constituidos por un doble enlace (benc�nico): un enlace com�n para todos los �tomos y un enlace particular para cada triada. Cada �tomo del grupo hexa est� unido por su lado exterior y con un enlace simple a otro grupo hexa formando una red carb�nica con todas sus posiciones de enlace ocupada.
Resumiendo, cada �tomos de carbono cede dos electrones para enlaces covalentes: uno para el n�cleo benc�nico y otro para la uni�n con otro grupo diferente. A cambio recibe seis �rbitas covalentes para sus tres enlaces (cada enlace covalente utiliza dos �rbitas comunes).