 + NaNO2 + 2HCl →(cool)→
+ NaNO2 + 2HCl →(cool)→ 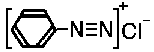 + NaCl + 2H2O
+ NaCl + 2H2O
−N=N−を「ジアゾ基」と言い、このジアゾ基を分子内に持つ化合物を、「アゾ化合物」と言います。
ジアゾ基は一般に不安定で、実在しないのですが、ベンゼン環に結合している場合に限り、不安定には違いないですが、存在出来ます。
ですからもっぱら、大学受験では、アリール・アゾ化合物(ベンゼン環にアゾ基が付いた化合物)を扱います。
アゾ化合物は一般に赤〜黄色の色を持っているため、染料として、世の中の役に立っています。
ベンゼン環を持つアゾ化合物は、一般に赤〜黄色の色を持っているため、染料として、世の中の役に立っています。
他の重要な例としては、フェノールフタレインもアゾ化合物です。だから赤色に染まるんですね。
話は脱線しますが学校の実験で、「指示薬(BTBやフェノールフタレイン、メチルオレンジ等)は、あまりいっぱい入れるな」と言われていると思いますが、なぜだか分かりますか?(これは有機ではなく無機の問題ですが・・・)
「もったいないから」
ま、それもありますが、そういう事ではなくて・・・。
ポイントは「指示薬自身のPH」ですよ。指示薬だって水溶液ですからPHがあります。ですからあまり加えすぎると、何のPHを測っているか(試料のPHなのか指示薬のPHなのか・・・)分からなくなるじゃないですか(^^)。
これはとても良く出題されますので、よくマスターして下さい。
というのも、化学に重要なフェノールの合成方法と、途中まで共通の反応経路を使うからでしょう。
 + NaNO2 + 2HCl →(cool)→
+ NaNO2 + 2HCl →(cool)→ 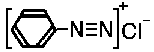 + NaCl + 2H2O
+ NaCl + 2H2O
アニリンのところで一度登場した反応と思いますが、この反応をもう一度考えて見てください。
結構珍しい反応ですね。
まず、「亜硝酸ナトリウム:NaNO2」が登場するのは、この反応くらいですね。
また加熱して反応させる事は多くても、この反応は冷却するんですね。
なぜ冷却するかといいますと、ジアゾニウムは不安定ですから、温度が上がると自然分解してしまうからなんです。(一般には、窒素分子N2を放出します)
それを逆手に取りまして、酸触媒を加えると加水分解が起き、
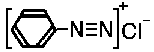 →
→ 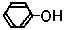 + N2
+ N2
とフェノールが生じます。これが重要なフェノールの製法の一つです。
これらの「塩化ベンゼンジアゾニウム」合成の反応過程は、極めて複雑なので、詳細に関しては、大学受験の範囲を大きく逸脱します。ですから結論だけを覚えて下さい。
どうしても途中過程を知りたい人のために、簡単にココに説明を付け足しました。
ちなみに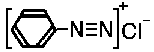 は、塩化ベンゼンジアゾニウムと言います。
は、塩化ベンゼンジアゾニウムと言います。
で、話を戻しましょう。
塩化ベンゼンジアゾニウムにナトリウムフェノラートを加えますと、
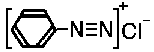 +
+ 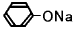 →
→ 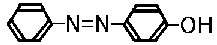 + NaCl
+ NaCl
こうして生じた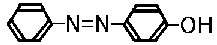 は「パラヒドロキシアゾフェノール」と言います。こいつはオレンジ色です。これも「アゾ化合物」の一種ですね。
は「パラヒドロキシアゾフェノール」と言います。こいつはオレンジ色です。これも「アゾ化合物」の一種ですね。
この反応を「(アゾ)カップリング」と言います。
芳香族のところで登場しましたアニリン が出てきましたが、この様にアンモニア分子の三つの水素のどれか(全部でも良い)をアルキル基で置換した化合物を「アミン」と言います。
が出てきましたが、この様にアンモニア分子の三つの水素のどれか(全部でも良い)をアルキル基で置換した化合物を「アミン」と言います。
(アミンの詳細は、大学で学んで下さい)