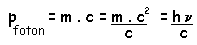Calor especifico de acuerdo a la Teoria cuantica
La hipótesis de estados de energía discretos para átomos y moléculas lleva a que el calor específico de una sustancia depende de la temperatura.
Cuando esta temperatura T es muy alta, y siendo K la
constante de Boltzman, el producto KT es mucho mayor que la separación entre estos niveles energéticos.
Las estimaciones clásicas y cuánticas difieren a temperaturas bajas.
como se forman los espectros moleculares
Los estados de energía en moléculas compuestas por dos átomos (llamadas moléculas diatómicas) están conformados por bandas correspondientes a la rotación molecular, superpuestas sobre los niveles correspondientes a la vibración molecular (con una separación mayor entre sí). Estos niveles vibracionales están a su vez superpuestos sobre los niveles correspondientes a la excitación de los electrones de los átomos que conforman la molécula (todavía más separados que los niveles vibracionales).
conductividad del agua
Los líquidos que contienen sustancias ionizadas conducen la electricidad.
Se ha determinado la conductividad específica del agua en condiciones que garanticen su pureza. El valor encontrado es de 0.038 . 10
-6 1/ Ohm cm.
El agua destilada común contiene impurezas que acrecientan su conductividad. Si se obtiene por destilación en contacto con aire, se halla que la conductividad específica ascenderá a 0.7 . 10
-6 1/ Ohm cm, aproximadamente 20 veces mayor que el valor mínimo hallado (correspondiente al agua pura).
descubrimiento del neutron
En el año 1930, Bothe (alemán, 1891-1957) y Becker bombardearon el boro y el berilio con partículas
a, produciendo una radiación muy penetrante, pero que no era afectada por campos eléctricos o magnéticos, de donde se dedujo que no estaba constituída por partículas cargadas, concluyendo erróneamente que se trataba de rayos gamma.
En 1932, Curie y Joliot observaron que cuando esta radiación pasaba a través de un material hidrogenado, se producían protones de energías elevadas (con una energía máxima de aproximadamente 7.5 MeV). Supusieron que los protones habían sido arrancados por el choque con los fotones gamma, conduciendo ésto a un
Efecto Compton nuclear.
Pero, con este rayo gamma, las ecuaciones de conservación del momento y de la energía que se plantean en el
Efecto Compton no se cumplían. Por esto, en el mismo año, el físico británico J. Chadwick (1891-1974) planteó, que, en lugar de radiación gamma, se emitían partículas neutras con masa muy similar a la de los protones, llamadas
neutrones .
Con estos elementos, Heisemberg (alemán, 1901-1976) propuso que el núcleo atómico puede estar conformado por dos clases de partículas (nucleones):
 protones (de carga positiva)
protones (de carga positiva)
 neutrones (de carga neutra)
neutrones (de carga neutra)
Estas dos clases de partículas son similares en masa:
masa en reposo del protón: mp 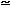 1.6725 x 10-27 Kg.
1.6725 x 10-27 Kg.
masa en reposo del neutrón: mn 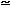 1.6748 x 10-27 Kg.
1.6748 x 10-27 Kg.
descubrimiento fenomenos de radiactividad
En el año 1896,
Becquerel observó que las sales de uranio tenían la propiedad de afectar una placa fotográfica a través de papel negro, y que además dotaban de una débil conductividad a los gases puestos en su contacto.
El uranio metálico y sus sales emitían, espontáneamente y por tiempo indeterminado, radiaciones semejantes a los rayos X y a los
rayos catódicos.
En 1898, G. C. Schmidt y
Marie Skladowska Curie encuentran, en forma independiente, las mismas propiedades en el torio. Marie Curie llama a estos elementos sustancias radiactivas y observa una gran actividad en minerales de uranio tales como:
- pechblenda (óxido de uranio)
- torianita (óxido de uranio y torio)
- calcolita (fosfato de cobre y uranio)
El matrimonio Curie descubre dos nuevos elementos mucho más activos que el uranio: el polonio y el bario. Más tarde se comienzan a descubrir más elementos radiactivos, reuniéndose en series o familias.
efecto compton
Cuando chocan un fotón y un electrón, puede ocurrir que el fotón ceda sólo una parte de su energía al electrón con que choca, disminuyendo la frecuencia. Si la energía del fotón antes del choque era de
E = hn (1) luego del choque será de: E = hn' (2)
con n' < n.
Se conoce a este efecto como efecto Compton.
Lo que Compton observó experimentalmente fue que cuando un elemento liviano, tal como el carbono, era atravesado por rayos X, se producía un fenómeno similar a la fluorescencia, pero en este caso, las longitudes de onda de los rayos dispersados luego del choque de la dirección y el sentido de la dispersión (en general, se suele decir que en el efecto Compton, la longitud de onda de la radiación dispersada depende del ángulo de dispersión).
Como observamos en el cambio de la energía de los fotones ( en las expresiones (1) y (2) ), se produce una disminución de la frecuencia, que es tanto más acentuada cuanto más marcado es el cambio que se experimenta en la dirección de dispersión. Así se concluye que el cambio en la dirección de propagación de la radiación incidente en el efecto Compton es proporcional a la cantidad de energía cedida a los electrones del medio con que choca.
efecto doppler
El efecto o corrimiento
Doppler relaciona la frecuencia que se mide de una onda con las velocidades relativas de:
- la fuente o transmisor.
- el medio.
- el receptor.
Cuando la fuente se aleja del receptor fijo, la frecuencia es menor. cuando la fuente se acerca al receptor fijo, la frecuencia es mayor. Ocurre lo mismo en el caso del receptor móvil y la fuente fija.
Para ondas sonoras se verifica:
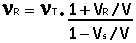
donde:
V : velocidad del sonido en el medio considerado en reposo.
V
s : velocidad de la fuente (positiva cuando esta se mueve hacia el receptor).
V
R : velocidad del receptor (positiva cuando se mueve hacia la fuente).
nT : frecuencia de la fuente o transmisor (medida por un observador en reposo respecto a la fuente).
nR : frecuencia medida por el receptor.
Tomemos Vs << V (supongamos VR = 0),
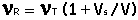
y
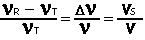
- Caso de ondas electromagnéticas (luz):
El efecto Doppler actúa de manera diferente, ya que este tipo de ondas no necesita un medio para propagarse.
efecto fotoelectrico
El vacío pierde sus propiedades de aislante entre dos electrodos conectados a una diferencia de potencial V cuando se ilumina el cátodo.
Cuando son iluminadas, las superficies metálicas pierden cargas negativas. Este es el
efecto fotoeléctrico, y se debe a que las radiaciones incidentes sobre un metal movilizan electrones.
Si las superficies metálicas están conectadas a un potencial negativo, rechazan los electrones liberados y, por lo tanto, pierden su carga.
En cambio, si están conectadas a un potencial positivo, "retienen" los electrones, conservando su carga.
La longitud de onda de la radiación incidente tiene un valor umbral para que se verifique este efecto, y de dicha longitud dependerá la velocidad de los electrones que son arrancados del metal.
Valores umbrales de l para diferentes materiales del cátodo | Material del cátodo | l [ m m ] |
| Carbono | 250 a 260 |
| Cesio | 370 a 700 |
| Plata | 300 a 500 |
| Rubidio | 600 |
| Sodio | 580 a 610 |
El número de electrones arrancados del material es proporcional al flujo de la radiación incidente.
En el efecto fotoeléctrico, el electrón que se desprende del metal absorbe toda la energía del fotón incidente. La máxima energía cinética de los electrones que escapan está dada por la fórmula de Einstein:
Ekmáx = h n - f0
donde:
h es la constante de Planck
n es la frecuencia incidente
f0 es la energía de arranque.
espectroscopia
Del latín spectrum (imagen) y del griego skopeio (observar). Es la parte de la Física que estudia los espectros.
Aunque actualmente el concepto espectro se ha extendido a campos muy diversos, incluso fuera de la Física, cuando se habla simplemente de Espectroscopía se sobrentiende que se alude al estudio del espectro electromagnético. Por tal motivo, la ESPECTROSCOPIA recibe diversos calificativos, según la región del espectro a que se refiere: espectroscopía gamma, de rayos X, ultravioleta, visible, infrarroja, de microondas, de ondas de radio. En cada uno de estos sectores, la espectroscopía encuentra unas aplicaciones características, teniendo en cuenta los agentes responsables de los correspondientes espectros.
Históricamente hay que remontarse a los tiempos de
Newton, verdadero padre de la espectroscopía, aunque, en realidad, sólo se comprendió la importancia y posibilidades de esta disciplina después de los trabajos de
Fraunhofer y, principalmente, de Bunsen y Kirchhoff. Ellos construyeron el primer espectroscopio realmente útil y, con su aplicación al análisis de materiales diversos, demostraron todo el poder de esta técnica.
espectroscopia atomica
En el campo atómico pueden distinguirse tres fases bien definidas en las aplicaciones de la
espectroscopía al conocimiento de la estructura de la materia. En primer lugar, la época de las series espectrales; más tarde la era de los multipletes, y, por último, la de interpretación de espectros muy complejos. Cada una de estas épocas va unida a un nombre especialmente famoso.
Niels Böhr representa el máximo exponente de la primera época, toda vez que, si bien las series espectrales fueron descubiertas y estudiadas empíricamente por Balmer, Paschen y otros, se debe a Böhr la gloria de haber relacionado directamente estas series con la estructura atómica, dando su modelo del átomo de hidrógeno en perfecto acuerdo con la estructura del correspondiente espectro observado en forma de series. Miguel A. Catalán descubrió en 1922 que los espectros de los átomos con varios electrones de valencia, junto a las series espectrales, presentaban grupos de líneas a las que se podía atribuir un origen común, tenían características semejantes y mostraban entre ellas relaciones perfectamente reconocibles. A estos grupos de líneas los denominó multipletes, y Sommerfeld demostró que se deben a transiciones entre estados electrónicos múltiples, producidos por la diversidad de estados cuánticos que pueden adquirir esos átomos. Este descubrimiento resultó equivalente al de Böhr, en cuanto permitió estudiar y explicar con detalle la estructura de los átomos mucho más complejos que el del hidrógeno y el de los elementos alcalinos, que eran los únicos que la teoría de Böhr explicaba satisfactoriamente, y dio gran impulso a la
espectroscopía atómica, de tal modo que ha permitido determinar prácticamente la estructura electrónica de todos los átomos conocidos.
Por último, Giulio Racah, desde el punto de vista teórico, revolucionó la
espectroscopía a partir de 1940 al demostrar que era posible calcular teóricamente, con bastante aproximación, la energía de los diversos estados electrónicos de cualquier átomo por complejo que fuera, lo que a su vez permite predecir su espectro y, por tanto, ha posibilitado extender las investigaciones espectroscópicas a átomos tales como las llamadas tierras raras y elementos transuránidos, que, desde un punto de vista simplemente empírico, eran inabordables en la práctica.
Espectroscopia de rayos X
Esta rama de la Espectroscopía estudia los espectros producidos cuando los electrones componentes de las capas internas de los átomos cambian sus estados cuánticos de energía.
El estudio espectroscópico de estos cambios permite averiguar la estructura y energía de esas capas internas de los electrones atómicos, y también puede aplicarse a problemas de reconocimiento analítico de sustancias, toda vez que el espectro de rayos X, como en general todos los espectros electromagnéticos de las sustancias, son una característica muy típica de las mismas.
En este campo merece recordarse la relación encontrada por
Moseley en 1912 entre la frecuencia de la radiación X absorbida por un átomo y su posición en el Sistema Periódico de los elementos químicos, lo que permitió descubrir el llamado número atómico y sentar las bases para una mejor comprensión de la estructura de la materia.
espectroscopia gamma
Esta parte de la ESPECTROSCOPIA estudia los espectros de radiación gamma producidos por los cambios energéticos que tienen lugar en el interior de los núcleos atómicos. Por tanto, este tipo de Espectroscopía tiene su principal aplicación en el estudio de la estructura y propiedades de dichos núcleos.
Actualmente, y gracias al descubrimiento del llamado efecto Mdssbauer, estas aplicaciones se han extendido al estudio del estado sólido, toda vez que se ha comprobado que los espectros, debido a este efecto, no son afectados por los átomos vecinos y permiten estudiar propiedades generales de todos los núcleos que componen un material sólido.
formacion de niveles atomicos
La Teoría Cuántica postula que la energía en los átomos está cuantizada, es decir, que depende de un número
n entero positivo.
Ahora bien, como los electrones en un átomo se mueven en un campo de fuerzas centrales, desde la presencia de un núcleo cargado positivamente, es de esperarse que el momento angular L también esté cuantizado.
Si consideramos L
2, éste dependerá del número cuántico l, que va desde cero hasta n-1, y de
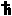
= h/2
p, donde h es la
constante de Planck, en la forma:
L2 = l ( l + 1 ) 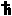 2
2 Se convino simbolizar la dependencia de l de la siguiente manera:
l 0 1 2 3 ...
símbolo s p d f ... Así, para n = 1, l = 0, formándose el estado 1s.
Para n = 2, l = 0, 1, formándose los estados 2s y 2p, y así sucesivamente.
Esquemáticamente, veamos los niveles para n = 1, 2, 3
n = 3 3s 3p 3d
n = 2 2s 2p
n = 1 1s
Se puede pasar de un nivel a otro por emisión o absorción de un fotón, respetando la regla: Dl = ±1.
fotones y presion de radiacion
En el año 1900 se observó, luego de la predicción teórica, que cuando un haz de luz se refleja en una superficie, ejerce una
presión: la luz y la radiación electromagnética en general, pueden ejercer presión al incidir sobre una superficie.
En 1906,
Albert Einstein demostró que la luz se comporta muchas veces como compuesta por un flujo de partículas cuando interactúa con la materia. Estas partículas son los cuantos de luz o fotones, que se mueven a velocidad c (como se convino en llamar a la velocidad de la luz, de 300.000 km/seg) siguiendo la dirección del haz. A través de este hecho se concluyó que la masa en reposo de los fotones debía ser cero.
La energía que tiene un fotón es E = h
n,
donde h es la
constante de Planck y
n es la
frecuencia de la luz.
El momento cinético para una partícula que tenga masa cero es p = m.v (donde m es la masa de la partícula, y v su velocidad), y su energía, m.c
2 (donde c, como se dijo antes, es la velocidad de la luz). Como habíamos dicho, en el caso del fotón, E = h
n, y su velocidad es c, por lo que
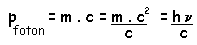
Imaginemos un haz de luz incidiendo sobre una superficie que es perpendicular (es decir, que forma un ángulo de 90ş) a la dirección del mismo. En un caso ideal en que el haz es totalmente reflejado (cuando la superficie no absorbe nada de la luz que le llega) los fotones chocan de manera elástica con la superficie. Si tenemos una cantidad n de fotones que chocan, por unidad de área, por segundo, el cambio de momento cinético por segundo será de 2nhn/c, y esta será la fuerza por unidad de área, que es la definición de presión:
P = 2nhn/c Si llamamos Q a nhn (que es la energía de la radiación que choca por unidad de área, por segundo), la presión de la radiación será, finalmente:
P = 2Q/c  La presión de la radiación y las colas de los cometas:
La presión de la radiación y las colas de los cometas:
Johannes Kepler afirmó que la presión de la luz solar forma las colas de los cometas. Se comprobó que esta presión influye en los cometas cuando la región activa solar está dirigida hacia ellos, impulsando la nube de polvo y gas que rodea al núcleo hacia el lado opuesto al Sol.
fusion y fision nuclear
En la
fisión nuclear, un núcleo fisionable (P.E. el 235U) captura un
neutrón y se rompe en dos partes emitiendo 2 o 3 neutrones.
Si, en valor medio, uno o más de los neutrones emitidos es capturado por otro núcleo fisionable produciendo una nueva fisión, estamos en presencia de una
reacción en cadena .
Cuando el núcleo se fisiona, libera la parte correspondiente a su energía de unión como rayos gamma.
La liberación de la energía de unión de un núcleo radiactivo puede producirse artificialmente en un reactor nuclear.
En una fusión nuclear se fusionan núcleos ligeros (P.E. 2H y 3H), liberándose energía.
Ocurre a temperaturas de aproximadamente 108 şK, ya que los iones pueden vencer la repulsión coulombiana sólo en este caso.
historia de la fisica
Desde los albores de la humanidad, el conocimiento de los fenómenos naturales se convirtió en una necesidad práctica que, a lo largo de los siglos, permitió acumular experiencia y conocimientos.
Intimamente ligada en sus comienzos a la filosofía, a las ciencias naturales y a la técnica empírica, la física no aparece como ciencia independiente hasta mediados del S XVI, cuando, con
Galileo, adquiere su dimensión experimental, que la caracterizará desde entonces. Si Galileo sentó las bases de la mecánica moderna, con su principio de inercia y con la ley de la caída de graves, el siglo siguiente contempló notables avances con el descubrimiento de las leyes de los gases por Boyle (inglés, 1626-1691), el invento del barómetro (Torricelli), la teoría ondulatoria de la luz, enunciada por Huygens y Hooke, y, muy especialmente, con el impulso dado por
Newton, verdadero creador de la física matemática, que enunció la ley de la gravitación universal y estudió los principios del movimiento.
Durante los Siglos XVIII y XIX se llevaron a cabo interesantes descubrimientos en el campo de la electricidad, el magnetismo y el estudio del calor, con físicos tan preclaros como
Volta, Clausius (alemán, 1822-1888), Helmholtz (alemán, 1821-1894), Ampčre, Maxwell y otros.
A finales del S XIX se inicia la llamada física moderna, con el
descubrimiento de la radiactividad (
Becquerel, 1896), que enlazó al inicio del siglo XX con las teorías cuánticas de
Planck y la de la relatividad de
Einstein.
Otros hitos importantes que merecen citarse en la historia reciente de la física son el descubrimiento de la radiactividad artificial (Joliot-Curie), el inicio de la era atómica con el primer reactor nuclear construido por Fermi (italiano, 1901-1954) en 1942, los modelos atómicos ideados por
Böhr y Sommerfeld (alemán, 1868-1951), la mecánica cuántica relativista elaborada por
Dirac y los estudios teóricos desarrollados por Heisenberg (alemán, 1901-1976).
Los temas que centran el interés de los físicos en los últimos años se refieren al hallazgo, estudio y sistematización de gran número de partículas subatómicas, la consecución de la
fusión nuclear controlada y el estudio del campo unitario que permita tratar de modo generalizado los distintos campos de fuerzas. En cuanto a su parcelación en diversas disciplinas, las más clásicas divisiones de la física son: la acústica, el electromagnetismo, la mecánica (estática, cinética y dinámica), la óptica y la termodinámica. No obstante, cabe señalar que es precisamente una característica de la física moderna la tendencia a buscar teorías generales que engloben en un único tratamiento teórico toda la complejidad del mundo físico.
Extraido de:
Enciclopedia Universal Multimedia de Planeta DeAgostini 1999.
interacciones entre particulas
Las interacciones entre partículas pueden ser de los siguientes tipos:
- Gravitacionales (de largo alcance).
- Electromagnéticas (también de largo alcance).
- Fuerzas entre cargas en reposo.
- Fuerzas entre cargas en movimiento.
- Efectos de campos de radiación magnéticos y eléctricos sobre un sistema de cargas.
- Débiles, responsables de la producción y el comportamiento de leptones (por ejemplo: en la
desintegración b) y de los procesos de desintegración de las partículas extrañas.
- Fuertes, entre las cuales aparecen las fuerzas nucleares, a las que se deben los enlaces entre nucleones.
principio de incertidumbre
Se puede representar un electrón como un paquete de ondas:
Y(x, t) donde x denota la posición y t el tiempo, mientras que Y representa la función de onda.
La posición más probable del electrón es el valor de x para el cual Y(x,t) es máximo.
Y(x,t) es proporcional a la probabilidad de que el electrón esté en x; además, Y(x,t) tiene un valor distinto de cero para el intervalo de valores de x, lo que hace que ocurra una incertidumbre del valor de la posición del electrón.
En 1927, Werner Heisenberg (alemán, 1901-1976), enunció el Principio de Incertidumbre.
Si Dx representa un rango de posiciones del electrón, o Dp, un rango de cantidades de movimiento, y
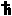 = h/(2p)
= h/(2p) donde h es la
constante de Planck,
Dx . Dp ~ 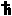 (1)
(1) También existe una indeterminación en determinar la energía E del electrón en un instante dado:
DE . Dt ~ 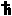 (2)
(2) Las ecuaciones (1) y (2) constituyen el enunciado del Principio de Incertidumbre. Más precisamente,
Dx . Dp ł ½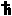
DE . Dt ł ½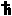
propiedades de la materia en estado solido
Los sólidos se caracterizan por el ordenamiento de forma regular de los átomos, con lo que las propiedades de los mismos se verán afectadas por los átomos vecinos. A partir de esta premisa se realiza el análisis de un sólido.
Llamamos estructura cristalina a la regularidad o periodicidad observada. Esta estructura se manifiesta en la red cristalina con la que distinguimos a cada sólido. Puede analizarse mediante el método de difracción de rayos X.
Según los enlaces que se observan, puede efectuarse la clasificación que presentamos en la tabla.
| Tipo de sólido | Características principales |
| Covalentes | - sus átomos se hallan ligados por enlaces direccionales, cuya orientación y naturaleza determina la red cristalina.
- son malos conductores de la electricidad y del calor, dado que no hay electrones libres que puedan ser utilizados como transporte.
|
| Cristales iónicos | - se forman a partir de un arreglo irregular de iones positivos o negativos, que aparecen por la transferencia de electrones de un átomo a otro.
- a temperaturas altas puede lograrse la conductividad, pero por lo general, estos cristales son malos conductores.
|
| Con enlaces de hidrógeno | - sus moléculas se hallan fuertemente polarizadas con uno o más átomos de hidrógeno (por ejemplo, el agua, H2O).
|
| Moleculares | - están constituidos por moléculas no polares, donde los electrones están todos apareados, de manera que no pueden formarse enlaces de tipo covalente.
- las moléculas están ligadas por las débiles
fuerzas de van der Waals, que provienen de la interacción de los dipolos eléctricos instantáneos originados por las configuraciones electrónicas de las moléculas.
|
| Metales | - sus energías de ionización son pequeñas.
- los electrones externos de los átomos se hallan ligados débilmente, con lo cual la red está compuesta por iones positivos y una nube de electrones que se mueven más o menos libremente. Esta es la razón por la que los metales son buenos conductores.
|
Bibliografía consultada: Física, volumen III: Fundamentos Cuánticos y Estadísticos, de M. Alonso y E. J. Finn (Addison - Wesley Iberoamericana, 1986).
radiacion sincroton
El principio de operación del sincrotón se usa en algunos aceleradores de alta energía, en regiones superiores de 1 GeV.
El sincrotón es un ciclotrón en el que o bien el campo magnético o bien la radiación o frecuencia aplicada se varía durante la aceleración, y en el que la fase de las partículas respecto al campo eléctrico de radio frecuencia se ajusta automáticamente al valor correcto de la aceleración.
El principio del sincrotón fue desarrollado por Vladimir Veksler (ruso, 1907-1966) y por Edwin McMillan (estadounidense, 1907-1991).
El aparato propuesto por Mc Millan (Physical Review, 68, 143, (1945)) hace uso de una estabilidad de fase que poseen ciertas órbitas del ciclotrón.
Sea una partícula cuya energía corresponde a una velocidad angular como para acoplarse a la frecuencia del campo eléctrico (energía de equilibrio) suponer que la partícula cruza los intervalos aceleradores en el momento justo en que el campo eléctrico se anula, cambiando de sentido tal que si la partícula llegara un poco antes resultaría acelerada.
Esta órbita es estacionaria.
Si se realiza un desplazamiento en la fase de modo que la partícula llega al gap demasiado pronto, resulta acelerada. El aumento de energía hace que la velocidad angular disminuya y el tiempo de llegada se retrase. Análogamente, un cambio de energía a partir del valor de equilibrio tiende a corregirse por sí mismo. Estas órbitas desplazadas continuarán oscilando, mientras su fase y energía varíen alrededor del equilibrio.
Para acelerar las partículas se cambia la energía de equilibrio, lo cual puede hacerse:
- variando el campo magnético.
- variando la frecuencia.
Mientras está cambiando la energía de equilibrio, la fase del movimiento se adelantará de modo de suministrar la fuerza aceleradora necesaria.
El aparato se llama sincrotón por su semejanza a la del motor síncrono. La radiación involucrada es la radiación sincrotón.
rayos x
En 1895, Röentgen encontró (experimentando con un tubo de
rayos catódicos o TRC) que los rayos que se generaban en el punto de incidencia de los rayos catódicos podían pasar a través de materiales normalmente opacos a la luz.
En un principio, como no conseguía con ellos formar espectros ópticos, ya sea de interferencia o de difracción y analizar así de qué tipo de radiación se trataba, los llamó
rayos X.
Sin embargo, en 1899, Hage y Wind observaron un ensanchamiento muy pequeño de un haz de rayos X luego de hacerlo pasar a través de unas rendijas con un ancho de milésimas de milímetro. Habían logrado la difracción de los rayos X, estimando luego que su longitud de onda era del orden de:
l x 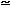 10-10 m = 1 Aş
10-10 m = 1 Aş
- Experiencia de Laue
Laue hizo incidir rayos X en un cristal, y observando la difracción ocurrida, postuló que, como la longitud de onda de los rayos X era del orden del espaciado de los átomos en un cristal, entonces éste podía utilizarse como una red tridimensional para la difracción X.
Teoria de bandas en materiales solidos
En un sólido los átomos se encuentran dispuestos de manera muy próxima, lo que ocasiona el desdoblamiento de los niveles de energía cuantizados individuales.
Este desdoblamiento origina
bandas de energía permitidas separadas por bandas prohibidas.
Un
conductor es un material en el cual la banda ocupada de energía más alta no está totalmente completa.
Si esta banda está llena y la siguiente banda permitida es grande en comparación con la cantidad
k.T (donde T es la temperatura y k la
constante de Boltzman)
el material es un
aislante.
Si el intervalo es pequeño, el material es un semiconductor intrínseco, en el que existen electrones en la banda de conducción.
Un superconductor es un material cuya resistencia llega a cero por debajo de cierta temperatura crítica. Este fenómeno es originado por una acción colectiva de los electrones.
żCómo se fabrica un semiconductor?
Se agregan impurezas que se clasifican en:
- materiales tipo n o dadores:
contribuyen al material original con niveles de energía llenos por debajo de la banda de conducción.
- materiales tipo p o receptores:
contribuyen con niveles de energía vacíos por encima de la banda de valencia llena del material.
teoria escalar de la difraccion
Sommerfeld (alemán, 1868-1951) definió la difracción como la propagación no rectilínea de la luz que no se puede interpretar a partir de las leyes de la reflexión y de la refracción.
Grimaldi, en el siglo XVII, fue el primero que observó fenómenos de difracción: al hacer pasar un haz de luz a través de una abertura practicada sobre una pantalla observó que, al proyectar el haz sobre otra pantalla, el paso de la zona iluminada a la zona de sombra no era abrupto (como indica la propagación rectilínea). Años después,
Fresnel realizó el primer intento serio de explicar los fenómenos de difracción (1818), basándose en unas modificaciones arbitrarias del principio de
Huygens. En 1882, Kirchhoff propuso la explicación de los fenómenos de difracción en términos de la teoría escalar. Su teoría tiene inconvenientes formales de orden matemático que fueron solucionados por Sommerfeld en 1894, introduciendo algunas modificaciones en la teoría anterior.
La teoría escalar es suficientemente rigurosa para explicar la mayor parte de los resultados experimentales macroscópicos. Pese a que se trata de una simplificación que no tiene en cuenta el carácter vectorial de los campos electromagnéticos, la teoría escalar funciona con éxito cuando las aberturas son más grandes que la longitud de onda de la luz y cuando las distancias de observación son suficientemente grandes. En estas condiciones, la polarización del campo electromagnético no es una información relevante y, por lo tanto, se puede prescindir del formalismo vectorial.
Diremos entonces que ocurre la difracción cuando un frente de ondas es interceptado por un obstáculo que limita su extensión.
![]()
![]()

 protones (de carga positiva)
protones (de carga positiva)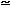 1.6725 x 10-27 Kg.
1.6725 x 10-27 Kg.