
3B属典型元素。両性元素。
イオン化傾向が水素より大きいため、融解電解を利用して精錬する。詳細は下参照。
ミョウバンの結晶、氷晶石に注意。
イオン化傾向が大きいにも関わらず、空気中で安定して存在出来るのは、表面にち密な酸化皮膜(Al2O3)ができ、内部を保護するためである。不動態を参照する事。
常温で水とは反応しないが、高温で水蒸気と反応して、酸化物になる。
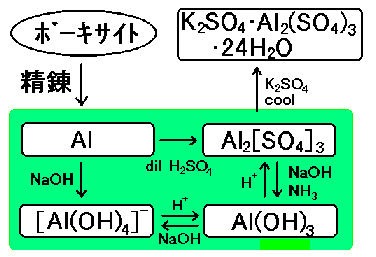
酸との反応:Al(OH)3 + 3HCl → AlCl3 + 3H2O
塩基との反応:Al(OH)3 + NaOH → [Al(OH)4]- + Na+
原料はボーキサイト。
イオン化傾向が大きいため、融解電解により精錬する。
融点を下げた方が精錬し易いため、凝固点降下剤として氷晶石(ひょうしょうせき)を加える。
氷晶石:Na3[AlF6]は覚えてね。

では、アルミの精練について説明しましょう。
アルミはイオン化傾向がとても大きいので、精練には他の金属よりも複雑な過程が必要になります。理屈をしっかり理解しなければ、とても覚えられる量ではないので、しっかり意味を押さえてください。
アルミの原料鉱石はボーキサイトです。ボーキサイトは多くの酸化アルミニウムを含むのでしたね。
で、酸化アルミ(ボーキサイト)から電解によってアルミの金属単体を取り出す訳ですが、なにせアルミは水(水素)よりもイオン化傾向が多いので、水溶液で電気分解しても、アルミは取り出せません。(やっても、陰極からはアルミではなく、水素ガスが発生します) そこで「融解電解」をするのでしたね。融解電解というのは、酸化アルミニウムを水溶液にせず、そのまま熱を加えて溶かし、電極棒を突っ込んで電解する方法でした。これならば、水素イオンがありませんので、水素が発生してしまい、アルミが析出しないという問題は起きません。
では、ボーキサイトを加熱して、電解すればよいのか?
それができたら楽なのですが、そう単純には行きません。
ボーキサイトは純粋な酸化アルミではなく、多くの不純物を含んでいます。例えば酸化鉄やケイ素等がかなり混じっています。
もしこの状態で直接融解電解しても、アルミは得られません。だって、鉄等の方がイオン化傾向が小さいから、そいつらが先に析出してしまいますから。
そこで何より先に、ボーキサイトから不純物を除いて、純粋な酸化アルミを作る必要があるのです。
融解電解の前にあるややこしい手順は、この「ボーキサイトから不純物をとりのぞくため」にあるのです。
では、その手順を説明しましょう。

まずボーキサイトに水酸化ナトリウムを加え、溶かします。
この状態でアルミはAl(OH)3の白い沈殿として底に溜まります。ただ、これにはFe(OH)3等、他の元素も混じります。それを取り除かなくてはなりませんね。
そこで、その沈殿を取り出して、更に濃い水酸化ナトリウムを加えます。すると、アルミは両性水酸化物ですから、[Al(OH)4]-になって再溶解します。ここで不純物のFe(OH)3等は、再溶解しませんので、底に沈んだままになります。で、沈殿を取り除けば、不純物は無くなります。こうして、アルミニウムイオンだけが溶けている水溶液ができました。
次に融解電解をする訳ですから、[Al(OH)4]-を酸化アルミにしなくてはなりません。その為には、水に溶けていてはどうにもならないので、一回沈殿させて、取り出さなくてはなりませんね。
そこで、再溶解の逆を行います。
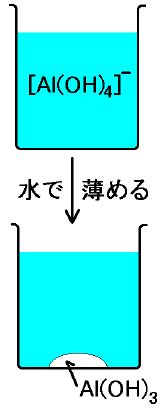
濃い塩基で再溶解して、薄ければ沈殿するのですから、アルミだけの水溶液になっているこの水溶液を水で薄め、PHを下げます(PH7に近づけます)。
すると[Al(OH)4]-はAl(OH)3となって沈殿します。
注意してください。先程も一度Al(OH)3の沈殿が出てきましたが、今度の沈殿は、意味が違います。最初の沈殿では、Fe(OH)3不純物を含みましたが、今度は不純物を含みません。一見無駄な操作をしている様ですが、不純物をとりのぞく為には、必要な操作なんですね。
で、沈んだAl(OH)3の沈殿を取り出します。
これを加熱しまして、水を飛ばします。
こうしますと、純粋な酸化アルミニウムが得られる訳です。
同じ酸化アルミニウムでも、ボーキサイトとは意味が違います。ボーキサイトは多くの不純物を含みますが、この段階での酸化アルミニウムは純粋です。この状態をアルミナと言います。
そこでこれに、凝固点降下剤として氷晶石を加えて加熱して、液体にします(要するにドロドロに溶かす訳ね)。後は電極棒を突っ込んで、電気分解してやれば、陰極にアルミニムが析出します。
これがアルミの精練です。