 + CH3COOH →
+ CH3COOH → 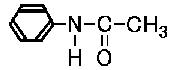 + H2O
+ H2O
アニリンのところで、カルボキシル基とアミノ基の反応をやりましたよね。
 + CH3COOH →
+ CH3COOH → 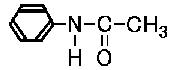 + H2O
+ H2Oいまは、一分子内に、カルボキシル基とアミノ基の両方があるのですよね。と言う事は、

とアミド結合により、繋がる事ができますよね。
抽象的な話だけでは眠くなると思うので、具体例を挙げてみましょう。アラニンとグルタミン酸を繋いでみますと・・・

こんな感じですね。
この様に、アミノ酸が二個合体した分子を「ジアミド」と言います。
ジアミドもやはり、カルボキシル基とアミド基の両方があるのですよね。
なら、まだ繋がる事ができますよね。これを何度も繰り返して、

長~い分子になれます。(デンプンを思い出そう)
こうしてできたのが「タンパク質」です。
ただ、一点気を付けたいのは、この「アミド結合」は、アミド結合とは言わないのです。「ペプチド結合」と言います。
「なんでやねん。アミド結合と何が違うねん?!」
と思うでしょう。確かに何の違いもありません。しかし、「タンパク質中のアミド結合は、特別にペプチド結合と言う」という(化学特有かつ、しばしば見かける)例外規則です。
化学は歴史が長い学問ですから、歴史的問題ってものがいろいろあるんです。ややこしいけど我慢知って下さい。
さて、タンパク質の消化は、中学理科によれば、
ですが、これで仕組が分かりましたね。タンパク質を加水分解した結果が、アミノ酸な訳です。
では、そのタンパク質の性質について、重要なものをいくつか検討してみましょう。
独学ための有機化学の「次のページ」へ:独学ための有機化学へ:目次へ