
CaSO4が難水溶性のため、たとえばCaCO3を硫酸に入れると、表面がCaSO4に覆われ、内部を保護するため、反応が進行しない。
なにせカルシウムは昔から人間生活と関わりが深いだけに、通称名が多い。一応覚える必要があります。
水酸化カルシウム。
水に溶かすと、いわゆる「石灰水」。二酸化炭素と反応して沈殿するのは、CaCO3を生じるため。
水酸化カルシウム水溶液。
二酸化炭素と反応して沈殿するのは、CaCO3を生じるため。
二酸化炭素を吸収してしまうので、保存する際には、ガラスビンにゴム栓をして保存する。
「ノリ(食べる方)」の中なんかに入っている「乾燥剤」がコレ。
石灰水に二酸化炭素を通じると生じる沈殿。炭酸カルシウムの事。
「しょう乳洞」を形作っているのがコレ。
アンモニアソーダ法の原料物質の一つ。
CaSO4硫酸カルシウム。
サラシ粉:CaCl(ClO)H2Oは、酸化剤として重要です。
半反応式は、
です。
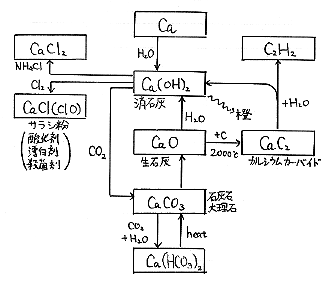
アルカリ土類金属の代表であるカルシウムは、われわれにとって大変身近な元素の一つであり、天然には、石灰石や大理石などの形で多量に存在、産出する。 しかし、その単体を得るためには、普通塩化カルシウムの融解電解法を用いる。こうして得られるカルシウムの単体は、常温でも水と反応する。生石灰は、石灰石を焼いてつくるが、この生石灰にコークスを混ぜて電気炉で強熱すると、カルシウムカーバイド(炭化カルシウム:CaC2)が得られる。カルシウムカーバイドは、水と反応させてアセチレンを発生させるのに用いる。また生石灰を水と反応させると生じる。 消石灰を塩化アンモニウムと反応させるとアンモニアを手軽に発生させる事ができる。
[慶應94医(一部変更)]