| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | H | He | ||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe |
| 6 | Cs | Ba | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra |
元素には103種類ありまして、それぞれ違った性質があります。 金は金色の固体金属で、柔らかく、反応性が弱く、電気を通します。 銅は十円玉の色の固体金属で、金よりも硬く、塩酸とは反応しませんが、硫酸とは反応します。 酸素は、常温で気体で無色。空気より重く、助燃作用があります。水にはあまり溶けません。窒素は・・・・・。
と、一つ一つの元素の性質を別々に考えると大変です。
幸い、103種類の元素はそれぞれ性質が違うのですが、似ている物のグループというものが存在します。
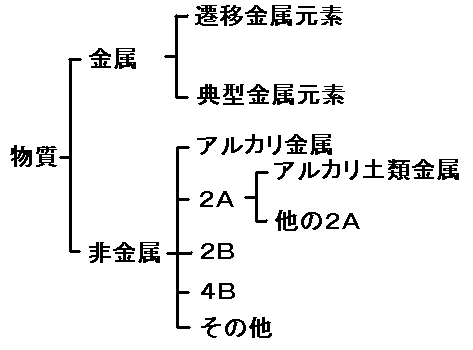
例えば金も銅も性質がかなり違いますが、金属である事には違いがありません。 酸素と窒素はかなり違いますが、非金属である事は共通しています。 このように似たものをグループを図にまとめると、こんな感じです。

全体は大きく「金属」と「非金属」に分けることができます。 周期表との関係を考えると、周期表の左の方が金属、右の方が非金属です。 教科書や参考書の周期表では、色分けされている事が多いと思います。(その他に半導体がありますが、それはまた後で述べます)
金属は金属結合する物質です。ナトリウムの結晶は、ナトリウム原子(正しくはナトリウムイオン)が、自由電子を共有することで、金属結合して存在します。
非金属とは基本的に、それ以外を指します。非金属同士は、共有結合でできています。塩素分子は、塩素原子二個が、共有結合で化合したものです。
金属と非金属が結合するには、イオン結合します。食塩(NaCl)は、金属であるナトリウムと、非金属の塩素が結合したものです。この場合、ナトリウムの価電子を、塩素が完全に奪って、静電気の力でくっついている物です。
金属はさらに、「典型金属元素」と「遷移金属元素」に分かれます。 周期表を習った時に、「周期表で縦に並んだ元素の性質は似ている」と習ったと思いますが、それがなり立たないのが「遷移元素」です。(典型元素では成り立ちます)
例えばナトリウムとカリウムは、周期表で縦に並んでいるので、性質が似ています。ですから「典型金属元素」です。しかし鉄とルテチルムは縦に並んでいますが、あまり似ていません。むしろ左右に並んだマンガンやコバルトに似ています。これが「遷移金属元素」です。 (なぜそうなるのかは、後で説明します。) では、「典型金属元素」「遷移金属元素」「非金属」に分けて、それぞれの性質について説明してみましょう。
さて、元素の性質としては、上の通りですが、化合物はさらに、それ特有の性質を持ちます。次に代表的な化合物をまとめてみましょう。